Конвертация единиц измерения концентрации
Содержание:
Формулы для пересчета концентраций растворов
В приводимой ниже таблице приняты следующие обозначения:
М — мольная масса растворенного вещества, г/моль; Э — эквивалентная масса растворенного вещества, г/моль; р — плотность раствора, г/мл.

* Дли жидкостей может применяться величина Pv, % (об.) —число миллилитров растворенной жидкости в 100 мл раствора.
РАСЧЕТНЫЕ ФОРМУЛЫ, ИСПОЛЬЗУЕМЫЕ ДЛЯ ПРИГОТОВЛЕНИЯ РАСТВОРОВ
Для приготовления определенного количества раствора какого-либо вещества заданной концентрации исходят из следующих данных: а) из количества чистого вещества и растворителя; б) из количества раствора данного вещества с более высокой концентрацией, чем заданная, и количества чистого растворителя или в) из количества двух растворов того же вещества, один из которых имеет концентрацию больше нужной, а другой — меньше.
Растворение вещества в воде
Пусть требуется приготовить А граммов раствора концентрации P . Тогда:
(I)
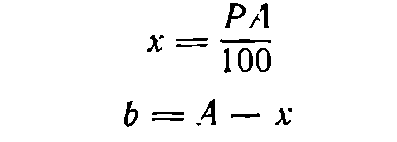
где х— необходимая масса растворяемого вещества, г; b—необходимая масса воды, г.
Если нужно приготовить определенный объем V раствора (в мл) концентрации Р, находят по таблицам плотность р (в г/см3) раствора данного вещества требуемой концентрации. Поскольку А = Vp, формула (1) будет иметь вид:
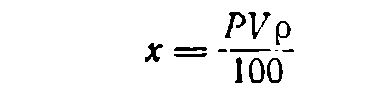
В тех случаях, когда растворяемое вещество представляет собой кристаллогидрат, т. е. содержит кристаллизационную воду, для расчета необходимого его количества используют формулу:
(4)
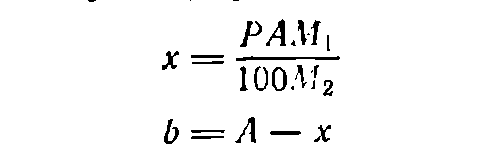
где х— необходимая масса кристаллогидрата, г; M1—мольная масса кристаллогидрата; М2—моль-мая масса вещества без кристаллизационной воды; b — необходимая масса воды, г.
Если нужно приготовить раствор объемом V (в мл) заданной нормальности N, вычисляют значение эквивалентной массы Э растворяемого вещества, после чего находят необходимую его навеску (в г) по формуле:
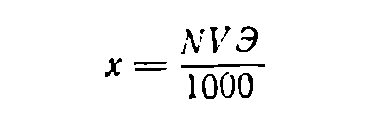
При приготовлении раствора заданной молярной концентрации применяют аналогичную формулу:
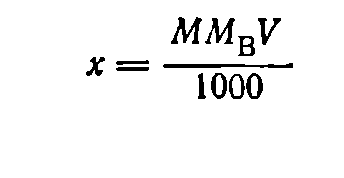
где М — молярная концентрация раствора; Мв — мольная масса растворяемого вещества; V — заданный объем раствора, мл.
Разбавление раствора водой
Пусть требуется приготовить раствор концентрации Р2 из имеющегося раствора с более высокой концентрацией Р1. Обозначим массу раствора до разбавления А1, а массу раствора после разбавления— А2. Тогда массу воды b (в г), необходимую для разбавления, находят по формуле (8) или (9) в зависимости от того, задано ли значение А\ или А2.
(9)
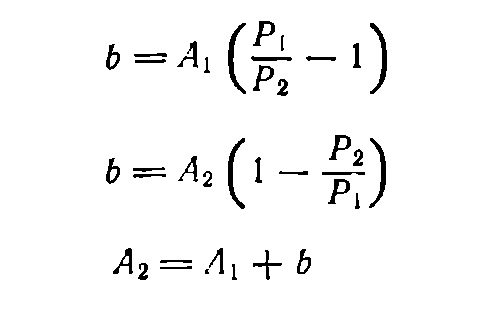
В тех случаях, когда известна не масса, а объем раствора, необходимо по таблицам найти плотности растворов данного вещества исходной и конечной концентраций — p1 и р2 соответственно. Тогда, если нужно приготовить раствор объемом V2 (в мл) концентрации Р2 , а концентрация исходного раствора равна P1 , то объем исходного раствора вычисляется по формуле:
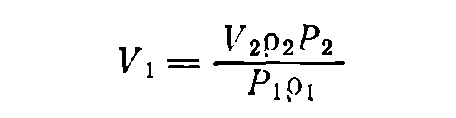
Объем воды (в мл) для разбавления: b = V2 — V1
Смешивание двух растворов различной концентрации
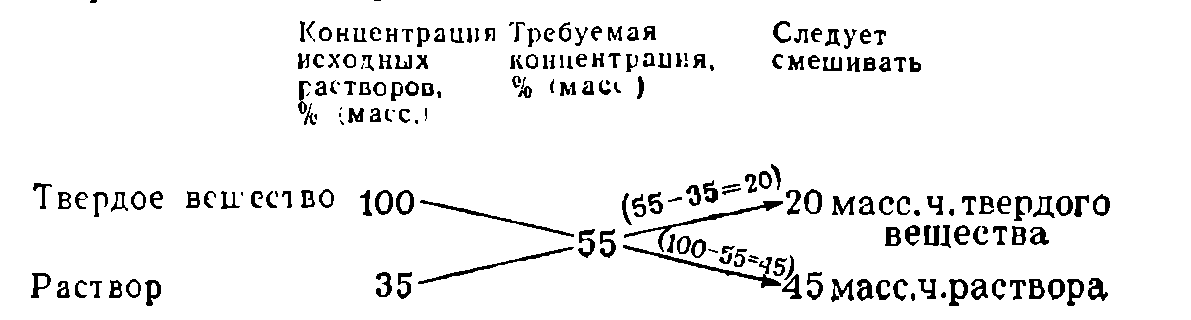
Пусть требуется приготовить раствор заданной концентрации из двух растворов того же вещества, один из которых имеет концентрацию больше нужной, а другой — меньше. Чтобы определить, в каких пропорциях следует смешивать растворы, пользуются «правилом креста», которое наглядно показано на следующем примере:
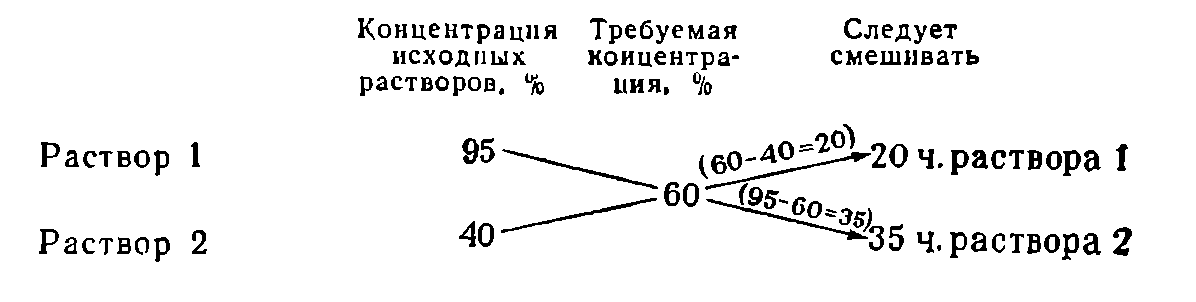
Смешиваемые растворы можно измерять в объемных или массовых частях в зависимости от того, в объемных или массовых процентах выражают концентрацию растворов.
«Правило креста» можно применять и в случаях разбавления раствора чистым растворителем. При этом концентрацию вещества в чистом растворителе считают равной нулю:

Для получения более концентрированного раствора растворением в нем дополнительного количества компонента твердое вещество условно считают раствором с концентрацией 100%:
Вычисление массовой доли спиртов в смеси этанола и метанола
Задача 189.
Для окисления смеси этанола и метанола в кислой среде потребовалось добавить 0,64 моль перманганата калия и при этом выделилось 8,96 л. газа. Вычислите массовые доли спиртов в исходной смеси.Решение:
1. Процессы окисления спиртов протекают по-разному:
5С₂H₅OH + 4KMnO₄ + 6H₂SO₄ = 5CH₃COOH + 4MnSO₄ + 2K2SO4 + 11H₂O5СH₃OH + 6KMnO₄ + 9H₂SO₄ = 5CО₂ + 6MnSO₄ + 3K₂SO4 + 19H₂O
2. Определим количество вещества СО2, образовавшегося при окислении метанола, получим:
n(СО2) = V(СО2)/Vm(СО2) = 8,96 л/22,4 л/моль = 0,4 моль.n(СH₃OH) = n(СО2) = 0,4 моль.m(СH₃OH) = 32 г/моль • 0,4 = 12,8 г.
3. Определим количество вещества KMnO₄, затраченное на окисление метанола получим:
n1(KMnO4) = 6/5n(СО2) = 1,2•0,4 = 0,48 моль.
4. Определим количество вещества KMnO₄, затраченное на окисление этанола получим:
n2(KMnO4) = n(KMnO4) — n1(KMnO4) = 0,64 — 0,48 = 0,16 моль.
Тогда
n(С₂H₅OH) = 5/4n(KMnO4) = 1,25 • 0,16 = 0,2 моль.
m(С₂H₅OH) = 46 г/моль • 0,2 = 9,2 г.
Отсюда
m(смеси) = 12,8 + 9,2 = + 22 г.
5. Вычислим массовые доли веществ, получим:
w%(СH₃OH) = /m(смеси) = (9,2 • 100%)/22 = 41,82%.
w%(С₂H₅OH) = 100% — 41,82 = 58,18%.
Ответ: w%(СH₃OH) = 41,82% • w%(С₂H₅OH) = 58,18%.
Определение объемных долей метана и этана в смеси газов
Задача 190.На сжигание природного газа объемом 200 л, содержащего метан, этан и негорючие примеси, затратили кислород объемом 395 л. Объемы газов измерены при нормальных условиях. Определите объемные доли метана и этана в газе, если объемная доля негорючих примесей составляет 5%.Решение:
1. Расчет объемов метана и этана в горючей смеси
Уравнения реакции горения веществ будут иметь вид:
1) CH4 + 2O2 = CO2 + 2H2O2) C2H6 + 3,5O2 = 2CO2 + 3H2O
Рассчитаем обем чистой газовой смеси, получим:
V(смеси) — 200 • (1 -0,05) = 190 л.
Из уравнений горения газов вытекает, что на сгорание 1 моль метана затрачивается 2 моль кислорода, а на сгорание этана — 3,5 моль.
Примем объм метана и этана в газовой смеси за «х» и «у» соответственно, 2х и 3,5Y.
Для вычисления состава смеси метана и этана в обьемных частях составим уравнение с двумя паременными, плоучим:
х + y = 190х + 3,5у = 395
Решим систему линейных уравнений методом подстановки:
Выразим из первого уравнения х + у = 190 данной системы «y» через «x», получим:
у = (190 — х).
Подставив во второе уравнение х + 3,5у = 395 данной системы вместо «y» выражение (19 — х), получим систему:
х + у = 190х + 3,5(190 — х) = 395
Полученные системы равносильны. В последней системе второе уравнение содержит только одну переменную. Решим это уравнение, получим:
х + 3,5(190 — х) = 395х + 665 — 3,5х = 395″х» = 108
Тогда
«у» = 190 — «х» = 190 — 108 = 82.
V(CH4) = 108 л;
V(C2H6) = 82 л.
2. Расчет объемных долей метана и этана в газе
w%V(CH4) = [V(CH4) • 100%]/V(смеси) = (108 л • 100%)/190 л = 56,84%;w%V(C2H6) = [V(C2H6) • 100%]/V(смеси) = (82 л • 100%)/190 л = 43,16%.
Ответ: w%V(CH4) = 56,84%; w%V(C2H6) = 43,16% л.
Как пользоваться EC- или TDS-метром?
Элементарно просто! Я ведь говорил, что эти приборы не сложнее градусника, правда? Сейчас вы в этом убедитесь.

• Снимите колпачок, защищающий электроды и погрузите их в раствор на глубину, не превышающую пунктирную линию.
• Чтобы провести замер в ёмкости, внутри которой табло EC-метра становится недоступно для считывания (например, в непрозрачной банке с узким горлом), в процессе замера нажмите кнопку HOLD (зафиксировать значение).
• Готово! Значение на табло обозначает концентрацию солей в вашем растворе. У TDS-метра оно отображается в ppm, у EC-метра — в миллисименсах на сантиметр (mS/cm) или микросименсах на сантиметр (uS/cm), в зависимости от модели.
ПРИЛОЖЕНИЕ 1 (обязательное)
ПРИЛОЖЕНИЕ 1ОбязательноеТаблица 1
Приведение объемов титрованных растворов при данной температуре к объемам при 20 °С (для 1000 см)
|
Температура, °C |
Вода, растворы молярной концентрации 0,01 моль/дм |
Растворы молярной концентрации |
||||
|
0,1 моль/дм (кроме ) |
0,5 моль/дм |
1 моль/дм |
0,5 моль/дм |
1 моль/дм |
||
|
5 |
+1,5 |
+1,7 |
+1,9 |
+2,3 |
+2,35 |
+3,6 |
|
6 |
+1,5 |
+1,65 |
+1,85 |
+2,2 |
+2,25 |
+3,4 |
|
7 |
+1,4 |
+1,6 |
+1,8 |
+2,15 |
+2,2 |
+3,2 |
|
8 |
+1,4 |
+1,55 |
+1,75 |
+2,1 |
+2,15 |
+3,0 |
|
9 |
+1,4 |
+1,5 |
+1,7 |
+2,0 |
+2,05 |
+2,7 |
|
10 |
+1,3 |
+1,45 |
+1,6 |
+1,9 |
+1,95 |
+2,5 |
|
11 |
+1,2 |
+1,35 |
+1,5 |
+1,8 |
+1,8 |
+2,3 |
|
12 |
+1,1 |
+1,3 |
+1,4 |
+1,6 |
+1,7 |
+2,0 |
|
13 |
+1,0 |
+1,1 |
+1,2 |
+1,4 |
+1,5 |
+1,8 |
|
14 |
+0,9 |
+1,0 |
+1,1 |
+1,2 |
+1,3 |
+1,6 |
|
15 |
+0,8 |
+0,9 |
+0,9 |
+1,0 |
+1,1 |
+1,3 |
|
16 |
+0,6 |
+0,7 |
+0,8 |
+0,8 |
+0,9 |
+1,1 |
|
17 |
+0,5 |
+0,6 |
+0,6 |
+0,6 |
+0,7 |
+0,8 |
|
18 |
+0,3 |
+0,4 |
+0,4 |
+0,4 |
+0,5 |
+0,6 |
|
19 |
+0,2 |
+0,2 |
+0,2 |
+0,2 |
+0,2 |
+0,3 |
|
20 |
0,0 |
0,0 |
0,0 |
0,0 |
0,0 |
0,0 |
|
21 |
-0,2 |
-0,2 |
-0,2 |
-0,2 |
-0,2 |
-0,3 |
|
22 |
-0,4 |
-0,4 |
-0,4 |
-0,5 |
-0,5 |
-0,6 |
|
23 |
-0,6 |
-0,6 |
-0,7 |
-0,7 |
-0,8 |
-0,9 |
|
24 |
-0,8 |
-0,9 |
-0,9 |
-1,0 |
-1,0 |
-1,2 |
|
25 |
-1,0 |
-1,1 |
-1,1 |
-1,2 |
-1,3 |
-1,5 |
|
26 |
-1,3 |
-1,4 |
-1,4 |
-1,4 |
-1,5 |
-1,8 |
|
27 |
-1,5 |
-1,7 |
-1,7 |
-1,7 |
-1,8 |
-2,1 |
|
28 |
-1,8 |
-2,0 |
-2,0 |
-2,0 |
-2,1 |
-2,4 |
|
29 |
-2,1 |
-2,3 |
-2,3 |
-2,3 |
-2,4 |
-2,8 |
|
30 |
-2,3 |
-2,5 |
-2,5 |
-2,6 |
-2,8 |
-3,2 |
Числа в графах 2-7 выражают объемы в кубических сантиметрах, которые следует прибавить (+) к 1000 см соответствующей жидкости при °С или вычесть (-) от 1000 см, чтобы получить объем титрованного раствора при 20 °С.Примеры
1. В колбу вместимостью 1 дм, калиброванную при 20 °C, необходимо налить при 15 °C раствор азотнокислого серебра 0,1 моль/дм. По табл.1 находим, что при 20 °C этот раствор займет объем больший на 0,9 см.
2. Из бюретки, калиброванной при 20 °С, при 25 °C израсходовано на титрование 34,75 см раствора гидроокиси натрия концентрации 1 моль/дм. При 20 °С расход реактива будет следующий:
см.
Таблица 2
Поправка объемов разбавленных растворов при разных температурах
|
Температура, °C |
Объем, см |
|||||
|
10 |
20 |
25 |
30 |
40 |
50 |
|
|
Поправка |
||||||
|
10 |
+0,01 |
+0,03 |
+0,03 |
+0,04 |
+0,05 |
+0,06 |
|
12 |
+0,01 |
+0,02 |
+0,03 |
+0,03 |
+0,04 |
+0,06 |
|
14 |
+0,01 |
+0,02 |
+0,02 |
+0,03 |
+0,04 |
+0,05 |
|
16 |
+0,01 |
+0,01 |
+0,02 |
+0,02 |
+0,03 |
+0,03 |
|
18 |
0,00 |
+0,01 |
+0,01 |
+0,01 |
+0,01 |
+0,02 |
|
20 |
0,00 |
0,00 |
0,00 |
0,00 |
0,00 |
0,00 |
|
22 |
0,00 |
-0,01 |
-0,01 |
-0,01 |
-0,02 |
-0,02 |
|
24 |
-0,01 |
-0,02 |
-0,02 |
-0,02 |
-0,03 |
-0,04 |
|
26 |
-0,01 |
-0,03 |
-0,03 |
-0,04 |
-0,05 |
-0,06 |
|
28 |
-0,02 |
-0,03 |
-0,04 |
-0,05 |
-0,07 |
-0,09 |
|
30 |
-0,02 |
-0,03 |
-0,05 |
-0,07 |
-0,09 |
-0,12 |
Табл.2 пользуются при работе с растворами концентрации 0,1 моль/дм или более разбавленными. ПРИЛОЖЕНИЕ 1. (Измененная редакция, Изм. N 1).
Примеры решения задач
Задача 1. Рассчитайте молярность, нормальность, моляльность, титр, мольную долю и мольное отношение для 40 мас.% раствора серной кислоты, если плотность этого раствора равна 1,303 г/см3.
Решение.
Масса 1 литра раствора равна М = 1000·1,303 = 1303,0 г.
Масса серной кислоты в этом растворе: m = 1303·0,4 = 521,2 г.
Молярность раствора См = 521,2/98 = 5,32 М.
Нормальность раствора Сн = 5,32/(1/2) = 10,64 н.
Титр раствора Т = 521,2/1000 = 0,5212 г/см3.
Моляльность μ = 5,32/(1,303 – 0,5212) = 6,8 моль/кг воды.
Обратите внимание на то, что в концентрированных растворах моляльность (μ) всегда больше молярности (См). В разбавленных растворах наоборот
Масса воды в растворе: m = 1303,0 – 521,2 = 781,8 г.
Количество вещества воды: n = 781,8/18 = 43,43 моль.
Мольная доля серной кислоты: χ = 5,32/(5,32+43,43) = 0,109. Мольная доля воды равна 1– 0,109 = 0,891.
Мольное отношение равно 5,32/43,43 = 0,1225.
Задача 2. Определите объём 70 мас.% раствора серной кислоты (r = 1,611 г/см3), который потребуется для приготовления 2 л 0,1 н раствора этой кислоты.
Решение.
2 л 0,1н раствора серной кислоты содержат 0,2 моль-экв, т.е. 0,1 моль или 9,8 г.
Масса 70%-го раствора кислоты m = 9,8/0,7 = 14 г.
Объём раствора кислоты V = 14/1,611 = 8,69 мл.
Задача 3. В 5 л воды растворили 100 л аммиака (н.у.). Рассчитать массовую долю и молярную концентрацию NH3 в полученном растворе, если его плотность равна 0,992 г/см3.
Решение.
Масса 100 л аммиака (н.у.) m = 17·100/22,4 = 75,9 г.
Масса раствора m = 5000 + 75,9 = 5075,9 г.
Массовая доля NH3 равна 75,9/5075,9 = 0,0149 или 1,49 %.
Количество вещества NH3 равно 100/22,4 = 4,46 моль.
Объём раствора V = 5,0759/0,992 = 5,12 л.
Молярность раствора См = 4,46/5,1168 = 0,872 моль/л.
Задача 4. Сколько мл 0,1М раствора ортофосфорной кислоты потребуется для нейтрализации 10 мл 0,3М раствора гидроксида бария?
Решение.
Переводим молярность в нормальность:
0,1 М Н3РО4 0,3 н; 0,3 М Ва(ОН)2 0,6 н.
Используя выражение (12), получаем: V(H3P04)=10·0,6/0,3 = 20 мл.
Задача 5. Какой объем, мл 2 и 14 мас.% растворов NaCl потребуется для приготовления 150 мл 6,2 мас.% раствора хлорида натрия?
Плотности растворов NaCl:
| С, мас.% | 2 | 6 | 7 | 14 |
| ρ, г/см3 | 2,012 | 1,041 | 1,049 | 1,101 |
Решение.
Методом интерполяции рассчитываем плотность 6,2 мас.% раствора NaCl:
6,2% =6% + 0,2(7% —6% )/(7 – 6) = 1,0410 + 0,0016 = 1,0426 г/см3.
Определяем массу раствора: m = 150·1,0426 = 156,39 г.
Находим массу NaCl в этом растворе: m = 156,39·0,062 = 9,70 г.
Для расчёта объёмов 2 мас.% раствора (V1) и 14 мас.% раствора (V2) составляем два уравнения с двумя неизвестными (баланс по массе раствора и по массе хлорида натрия):
156,39 = V1 1,012 + V2 1,101 ,
9,70 = V1·1,012·0,02 + V2·1,101·0,14 .
Решение системы этих двух уравнений дает V1 =100,45 мл и V2 = 49,71 мл.
Задачи для самостоятельного решения
3.1. Рассчитайте нормальность 2 М раствора сульфата железа (III), взаимодействующего со щёлочью в водном растворе.
12 н.
3.2. Определите молярность 0,2 н раствора сульфата магния, взаимодействующего с ортофосфатом натрия в водном растворе.
0,1 M.
3.3. Рассчитайте нормальность 0,02 М раствора KMnO4, взаимодействующего с восстановителем в нейтральной среде.
0,06 н.
3.4. Определите молярность 0,1 н раствора KMnO4, взаимодействующего с восстановителем в кислой среде.
0,02 M.
3.5. Рассчитать нормальность 0,2 М раствора K2Cr2O7, взаимодействующего с восстановителем в кислой среде.
1,2 M.
3.6. 15 г CuSO4·5H2O растворили в 200 г 6 мас.% раствора CuSO4. Чему равна массовая доля сульфата меди, а также молярность, моляльность и титр полученного раствора, если его плотность составляет 1,107 г/мл?
0,1; 0,695М; 0,698 моль/кг; 0,111 г/мл.
3.7. При выпаривании 400 мл 12 мас.% раствора KNO3 (плотность раствора 1,076 г/мл) получили 2М раствор нитрата калия. Определить объём полученного раствора, его нормальную концентрацию и титр.
255 мл; 2 н; 0,203 г/мл.
3.8. В 3 л воды растворили 67,2 л хлороводорода, измеренного при нормальных условиях. Плотность полученного раствора равна 1,016 г/мл. Вычислить массовую, мольную долю растворённого вещества и мольное отношение растворённого вещества и воды в приготовленном растворе.
0,035; 0,0177; 1:55,6.
3.9. Сколько граммов NaCl надо добавить к 250 г 6 мас.% раствору NaCl, чтобы приготовить 500 мл раствора хлорида натрия, содержащего 16 мас.% NaCl? Плотность полученного раствора составляет 1,116 г/мл. Определить молярную концентрацию и титр полученного раствора.
74,28 г; 3,05 М; 0,179 г/мл.
3.10. Определить массу воды, в которой следует растворить 26 г ВaCl2·2H2O для получения 0,55М раствора ВaCl2 (плотность раствора 1,092 г/мл). Вычислить титр и моляльность полученного раствора.
192,4 г; 0,111 г/мл; 0,56 моль/кг.
Связанные количества
Для описания состава смеси можно использовать несколько других величин
Обратите внимание, что это не следует называть концентрациями.
Нормальность
Нормальность определяется как молярная концентрация, деленная на коэффициент эквивалентности . Поскольку определение фактора эквивалентности зависит от контекста (какая реакция изучается), IUPAC и NIST не одобряют использование нормальности.
cя{\ displaystyle c_ {i}}жеq{\ displaystyle f _ {\ mathrm {eq}}}
Моляльность
(Не путать с молярностью )
Моляльность раствора определяется как количество составляющего (в молях), деленное на массу растворителя (а не на массу раствора):
бя{\ displaystyle b_ {i}}пя{\ displaystyle n_ {i}}мsолvепт{\ displaystyle m _ {\ mathrm {растворитель}}}
- бязнак равнопямsолvепт.{\ displaystyle b_ {i} = {\ frac {n_ {i}} {m _ {\ mathrm {растворитель}}}}.}
Единица СИ для моляльности является моль / кг.
Мольная доля
Мольная доля определяется как количество компонента (в молях), деленное на общее количество всех компонентов в смеси :
Икся{\ displaystyle x_ {i}}пя{\ displaystyle n_ {i}}птот{\ displaystyle n _ {\ mathrm {tot}}}
- Иксязнак равнопяптот.{\ displaystyle x_ {i} = {\ frac {n_ {i}} {n _ {\ mathrm {tot}}}}.}
Единица СИ является моль / моль. Однако устаревшее обозначение частей на единицу часто используется для описания малых мольных долей.
Молярное отношение
Молярное соотношение определяется как количество компонента, деленное на общее количество всех других компонентов в смеси:
ря{\ displaystyle r_ {i}}пя{\ displaystyle n_ {i}}
- рязнак равнопяптот-пя.{\ displaystyle r_ {i} = {\ frac {n_ {i}} {n _ {\ mathrm {tot}} -n_ {i}}}.}
Если намного меньше , мольное отношение почти идентично мольной доле.
пя{\ displaystyle n_ {i}}птот{\ displaystyle n _ {\ mathrm {tot}}}
Единица СИ является моль / моль. Однако устаревшее обозначение частей на единицу часто используется для описания малых мольных соотношений.
Массовая доля
Массовая доля — это отношение массы одного вещества к массе всей смеси , определяемое как:
шя{\ displaystyle w_ {i}}мя{\ displaystyle m_ {i}}мтот{\ Displaystyle м _ {\ mathrm {tot}}}
- шязнак равномямтот.{\ displaystyle w_ {i} = {\ frac {m_ {i}} {m _ {\ mathrm {tot}}}}.}
Единица СИ является кг / кг. Однако устаревшее обозначение частей на единицу часто используется для описания малых массовых долей.
Соотношение масс
Массовое отношение определяется как масса компонента, деленная на общую массу всех других компонентов в смеси:
ζя{\ displaystyle \ zeta _ {я}}мя{\ displaystyle m_ {i}}
- ζязнак равномямтот-мя.{\ displaystyle \ zeta _ {i} = {\ frac {m_ {i}} {m _ {\ mathrm {tot}} -m_ {i}}}.}
Если намного меньше , массовое отношение почти идентично массовой доле.
мя{\ displaystyle m_ {i}}мтот{\ Displaystyle м _ {\ mathrm {tot}}}
Единица СИ является кг / кг. Однако устаревшее обозначение частей на единицу часто используется для описания небольших массовых соотношений.
Что такое концентрация
Концентрация относится к тому, сколько вещества присутствует в смеси. Как правило, это выражается в единицах объема смеси. Например,
Массовая концентрация показывает, какую массу вещества составляет в единице объема смеси. Это может быть получено путем деления массы вещества на общий объем смеси. Например, если вы растворяете 5,00 г чистой поваренной соли (NaCl) в воде, чтобы получить раствор соли 100 см.3тогдаконцентрация соли в растворе 5,0 кг-3, Как правило, в химических экспериментах концентрации выражаются в г см.-3.
Молярная концентрация дает количествомоль вещества на единицу объема в смеси. Например, давайте возьмем солевой раствор, описанный выше. Моль NaCl имеет массу 58,5 г. Это означает, что для вышеуказанного решения должно быть 855 молей на 1 м.3 решения. Следовательно, концентрацию можно охарактеризовать как 855 моль м.-3, Как правило, химики используют единицы мол дм-3 особенно при обсуждении концентрации газов. Моль на литр часто обозначается символом М. В 2 М растворе HCl содержится 2 моль HCl, растворенного в 1 л раствора.
Объемная концентрация показывает, сколько объема раствора занимает вещество. Это может быть выражено в процентах. Проценты также используются, чтобы выразить, сколько измасса раствора учитывается веществом. Например, 1% раствор глюкозы содержит 1 г глюкозы, растворенной в 99 г воды.
Часто концентрации также приведены как частей на миллион (промилле) или же частей на миллиард (ppb), Эти типы измерений показывают, сколько молекул вещества присутствует на один миллион / один миллиард молекул смеси. Например, приведенный ниже график показывает, как концентрация диоксида углерода в нашей атмосфере увеличилась за последние несколько десятилетий:

Изменение содержания углекислого газа в атмосфере с концентрацией в миллионных долях, показанной по оси Y, и года, показанного по оси X.
Словаконцентрированный а такжеразбавлять часто используются для указания относительных концентраций раствора. Вот,концентрированный относится к более высокой концентрации в то время как разбавлять относится к более низкой концентрации.
Способы выражения концентрации растворов
Существуют различные способы выражения концентрации растворов.
Массовая доля ω компонента раствора определяется как отношение массы данного компонента Х, содержащегося в данной массе раствора к массе всего раствора m. Массовая доля – безразмерная величина, её выражают в долях от единицы:
ωр.в. = mр.в./mр-ра(0 < ωр.в. < 1) (1)
Массовый процент представляет собой массовую долю, умноженную на 100:
ω(Х) = m(Х)/m · 100% (0% < ω(Х) < 100%) (2)
где ω(X) – массовая доля компонента раствора X; m(X) – масса компонента раствора X; m – общая масса раствора.
Мольная доля χ компонента раствора равна отношению количества вещества данного компонента X к суммарному количеству вещества всех компонентов в растворе.
Для бинарного раствора, состоящего из растворённого вещества Х и растворителя (например, Н2О), мольная доля растворённого вещества равна:
χ(X) = n(X)/(n(X) + n(H2O)) (3)
Мольный процент представляет мольную долю, умноженную на 100:
χ(X), % = (χ(X)·100)% (4)
Объёмная доля φ компонента раствора определяется как отношение объёма данного компонента Х к общему объёму раствора V. Объёмная доля – безразмерная величина, её выражают в долях от единицы:
φ(Х) = V(Х)/V (0 < φ(Х) < 1) (5)
Объёмный процент представляет собой объёмную долю, умноженную на 100.
φ(X), % = (φ(X)·100)%
Молярность (молярная концентрация) C или Cм определяется как отношение количества растворённого вещества X, моль к объёму раствора V, л:
Cм(Х) = n(Х)/V (6)
Основной единицей молярности является моль/л или М. Пример записи молярной концентрации: Cм(H2SO4) = 0,8 моль/л или 0,8М.
Нормальность Сн определяется как отношение количества эквивалентов растворённого вещества X к объёму раствора V:
Cн(Х) = nэкв.(Х)/V (7)
Основной единицей нормальности является моль-экв/л. Пример записи нормальной концентрации: Сн(H2SO4) = 0,8 моль-экв/л или 0,8н.
Титр Т показывает, сколько граммов растворённого вещества X содержится в 1 мл или в 1 см3 раствора:
T(Х) = m(Х)/V (8)
где m(X) – масса растворённого вещества X, V – объём раствора в мл.
Моляльность раствора μ показывает количество растворённого вещества X в 1 кг растворителя:
μ(Х) = n(Х)/mр-ля (9)
где n(X) – число моль растворённого вещества X, mр-ля – масса растворителя в кг.
Мольное (массовое и объёмное) отношение – это отношение количеств (масс и объёмов соответственно) компонентов в растворе.
Необходимо иметь ввиду, что нормальность Сн всегда больше или равна молярности См. Связь между ними описывается выражением:
См = Сн · f(Х) (10)
Для получения навыков пересчёта молярности в нормальность и наоборот рассмотрим табл. 1. В этой таблице приведены значения молярности См, которые необходимо пересчитать в нормальность Сн и величины нормальности Сн, которые следует пересчитать в молярность См.
Пересчёт осуществляем по уравнению (10). При этом нормальность раствора находим по уравнению:
Сн = См/f(Х) (11)
Результаты расчётов приведены в табл. 2.
Таблица 1. К определению молярности и нормальности растворов
| Тип химического превращения | См | Сн | Сн | См |
| Реакции обмена | 0,2 M Na2SO4 | ? | 6 н FeCl3 | ? |
| 1,5 M Fe2(SO4)3 | ? | 0,1 н Ва(ОН)2 | ? | |
| Реакции окисления-восстановления |
0,05 М KMnO4
в кислой среде |
? |
0,03 М KMnO4
в нейтральной среде |
? |
Таблица 2
Значения молярности и нормальности растворов
| Тип химического превращения | См | Сн | Сн | См |
| Реакции обмена | 0,2M Ma2SO4 | 0,4н | 6н FeCl3 | 2М |
| 1,5M Fe2(SO4)3 | 9н | 0,1н Ва(ОН)2 | 0,05М | |
| Реакции окисления-восстановления | 0,05М KMnO4 в кислой среде | 0,25н |
0,03М KMnO4
в нейтральной среде |
0,01М |
Между объёмами V и нормальностями Сн реагирующих веществ существует соотношение:
V1 Сн,1 =V2 Сн,2 (12)
Растворы. Способы выражения концентрации
Истинными
растворами называются гомогенные системы, состоящие из двух или
большего числа компонентов, состав которых может непрерывно
меняться в определенных пределах.
Агрегатное состояние растворов может быть твердым, жидким или
газообразным. Обычно термин “растворы” относят к жидким
системам. Компонент раствора, имеющий то же агрегатное
состояние, что и раствор, называют растворителем, остальные
компоненты – растворенными веществами. Это деление достаточно
условно, например в растворе, компонентами которого являются
азотная кислота и вода, растворителем и растворенным веществом
можно считать каждый из компонентов. Подобные растворы называют
взаимными, например взаимный раствор азотной кислоты и воды.
Однако в случае, когда одним из компонентов раствора является
вода, ее традиционно считают растворителем.
Содержание растворенного вещества в растворе
может быть выражено несколькими способами:
Массовая доля растворенного вещества:
отношение массы растворенного вещества к массе раствора:
где – массовая доля
растворенного вещества, – масса
растворенного вещества, – масса
раствора. Это частный случай определения массовой доли.
Концентрация (молярная концентрация,
молярность): отношение количества растворенного вещества
к объему раствора V:
Молярная концентрация имеет принятую в химии размерность
[моль/л], которая часто обозначается М и называется молярностью.
Например, концентрация раствора 5 моль/л может быть записана как
5 М и такой раствор называется пятимолярным.
Эквивалентная (нормальная)
концентрация: отношение количества эквивалентов
растворенного вещества ЭКВ к
объему V раствора:
Эквивалент – это реальная или
условная частица вещества, которая в данной кислотно-основной
реакции эквивалента (равна) одному иону водорода или в данной
окислительно-восстановительной реакции – одному электрону.
Например в реакции
H2SO4 = K2SO4 +
2H2O
эквивалентом
гидроксида калия будет молекула КОН, а серной кислоты молекулы H2SO4.
Фактор эквивалентности
fЭКВ показывает, какая доля реальной частицы
данного вещества в данной кислотно-основной реакции эквивалента
(равна) одному иону водорода или в данной
окислительно-восстановительной реакции – одному электрону.
Для приведенного примера
1
1/2
Величина, обратная фактору
эквивалентности, называется эквивалентным числом
zB:
Число частиц эквивалентов вещества
NЭ связано с числом реальных частиц N
соотношением:
Количество вещества эквивалента
равно отношению числа частиц эквивалентов к числу Авогадро:
Молярная масса эквивалента равна отношению массы вещества к
количеству вещества эквивалента:
и имеет
размерность г/моль.
Эквивалентная
концентрация имеет размерность [моль эквивалента/л] и называется
также нормальной концентрацией или нормальностью раствора и
обозначается н. Например, раствор с эквивалентной
концентрацией 0,5 моль-эквивалентов/л называется полунормальным,
его концентрация запишется 0,5 н.
Молярная концентрация и массовая доля
растворенного вещества связаны между собой. Предположим, что мы
знаем массовую долю растворенного вещества , плотность раствора и молярную массу растворенного вещества М. В качестве
вспомогательной величины возьмем объем раствора V. Тогда масса
раствора :
масса
растворенного вешества:
количество растворенного
вещества:
Подставляем выражение для количества
растворенного вещества в формулу для концентрации и сокращаем
объем раствора V:
Если из полученного соотношения
выразить массовую долю растворенного вещества, то:
Оба выражения (для концентрации и массовой доли) содержат
размерные величины, поэтому подстановка числовых значений
требует от них определенных размерностей: С[моль/л], М[г/моль],
[г/л]. Для перевода плотности из
размерности [г/мл] необходимо числовое значение умножить на
1000:
[г/л] = [г/мл]•1000
Примеры
- 11,6 г NaCl растворяют в 100 г воды. Конечная массовая концентрация ρ (NaCl) равна
- ρ (NaCl) =11,6 г11,6 г + 100 г = 0,104 г / г = 10,4%.
Плотность такого раствора составляет 1,07 г / мл, поэтому его объем равен
- V = 11,6 г + 100 г1,07 г / мл = 104,3 мл.
Следовательно, молярная концентрация NaCl в растворе составляет
- с (NaCl) =11,6 г58 г / моль / 104,3 мл = 0,00192 моль / мл = 1,92 моль / л.
Здесь 58 г / моль — молярная масса NaCl.
- Типичной задачей химии является приготовление 100 мл (= 0,1 л) раствора NaCl в воде с концентрацией 2 моль / л. Необходимая масса соли составляет
- m (NaCl) = 2 моль / л × 0,1 л × 58 г / моль = 11,6 г.
Для создания раствора в мерную колбу помещают 11,6 г NaCl , растворяют в небольшом количестве воды, затем добавляют еще воды, пока общий объем не достигнет 100 мл.
- Плотность воды составляет примерно 1000 г / л, а ее молярная масса составляет 18,02 г / моль (или 1 / 18,02 = 0,055 моль / г). Следовательно, молярная концентрация воды равна
- с (Н 2 О) =1000 г / л18,02 г / моль ≈ 55,5 моль / л.
Аналогичным образом, концентрация твердого водорода (молярная масса = 2,02 г / моль) равна
- с (Н 2 ) =88 г / л2,02 г / моль = 43,7 моль / л.
Концентрация чистого четырехокиси осмия (молярная масса = 254,23 г / моль) составляет
- с (OsO 4 ) =5,1 кг / л254,23 г / моль = 20,1 моль / л.
-
Типичный белок в бактериях , таких как E. coli , может иметь около 60 копий, а объем бактерии составляет около 10-15 л. Таким образом, числовая концентрация C равна
C = 60 / (10 -15 л) = 6 × 10 16 л -1 .
Молярная концентрация
- c =CN A знак равно 6 × 10 16 л −16 × 10 23 моль -1= 10-7 моль / л = 100 нмоль / л.
-
Референсные диапазоны для анализов крови , отсортированные по молярной концентрации: