Популярная библиотека химических элементов
Содержание:
Калий: что нужно знать о нем

Замены для этого щелочного нутриента не существует. При недостатке микроэлемента нарушаются функции сердца, почек, мозга, мышечных тканей. Калий контролирует водный и электролитный баланс, регулирует показатели осмотического давления в клетках. В союзе с натрием и магнием нутриент нормализует показатель pH в жидкостных средах.
В больших количествах нутриент находится в растительной пище. Источниками калия для организма являются овощные культуры, фрукты и ягоды. Полуфабрикаты, блюда быстрого приготовления и прочая нерациональная еда создают дефицит щелочного нутриента.
В организме хранится примерно 250 г минерала. Кровь забирает 3 г вещества, остальное количество распределяется по клеткам. Для пополнения запасов ежедневно с едой в организм должно поступать 3-5 г калия.
При двигательной активности, тяжелой работе, спортивных тренировка потребность в калии возрастает. Чем сильнее физическая нагрузка, тем больше необходимо включать в рацион продуктов, в которых находится калий. Повышенное количество минерала нужно при употреблении мочегонных препаратов, обильном потоотделении и беременности.
Полезные свойства калия
Благодаря калию все органы и системы в человеческом организме работают слаженно. Минерал выполняет целый ряд функций:

- Нормализует давление. Нутриент возвращает сосудам эластичность, не дает закрепляться холестериновым бляшкам на их стенках. Беспрепятственная циркуляция крови позволяет давлению оставаться в норме. На начальной стадии гипертонии врачи рекомендуют пациентам употреблять продукты питания богатые калием.
- Налаживает функционирование почек. Микроэлемент, понижая кислотность крови, уменьшает риск образования камней в почках. Пациентам с почечной недостаточностью употреблять в пищу, обогащенную щелочным нутриентом, противопоказано. У них велика вероятность появления гиперкалиемии.
- Устраняет избыточную жидкость. Микроэлемент нормализует водный баланс, регулирует массу тела.
- Увеличивает скорость метаболизма. При нехватке калия в организме замедляются обменные процессы. Жиры перестают расщепляться, откладываются в подкожной клетчатке.
- Бережет от стрессов. Продукты, содержащие хлор, натрий и калий, улучшают работу нервных корешков и мышечных клеток. Благодаря им налаживается передача нервных импульсов. Мозговые центры дают адекватную ответную реакцию на раздражители. У человека проходит нервозность, тревожность, бессонница.
- Устраняет спазмы мышц. При нехватке нутриента возникают спазмы и судороги. Даже минимальный дефицит калия вызывает мышечные боли.
- Укрепляет костные ткани. Нутриент предупреждает развитие остеопороза, патологий суставов и позвоночника.
- Стимулирует работу головного мозга. Минерал обеспечивает мозговые клетки кислородом. При его нехватке развивается гипоксия, сопровождающаяся снижением интеллектуальных способностей, утратой памяти, рассеянностью.
- Перерабатывает сахара в энергию. При дефиците нутриента перестает расщепляться глюкоза, и вырабатываться энергия. При пониженной концентрации калия человек быстро утомляется, теряет работоспособность.
Мед – идеальный поставщик нутриентов и энергии. Медицинские исследования подтверждают, что в меде содержится калий, а также натрий, фосфор, магний, хлор – минералы, усиливающие полезное действие K.

Таблица № 1
| Минерал | Количество, мг |
| Калий | 36 |
| Хлор | 19 |
| Фосфор | 18 |
| Натрий | 10 |
| Магний | 3 |
Что приводит к дефициту калия
Недостаток микроэлемента возникает:
- Если человек принимает мочегонные препараты, не удовлетворяя потребность в калии.
- Когда содержание калия в основных продуктах питания снижено, а натрия – повышено (велико количество соли и добавок, включающих этот минерал).
- При введении в рацион большого количества продуктов питания без калия (фаст-фуд).
- Чрезмерная двигательная активность, завышенные физические нагрузки.
- Курение и алкоголь (даже если человек мало привержен к вредным привычкам).
- Употребление наркотиков (в небольших, тем более в повышенных, дозах).
Симптомы недостатка калия

Определить нехватку нутриента без лабораторных исследований сложно. Симптоматика многих заболеваний и дефицита минерала совпадает. Если человек питается в основном продуктами, обедненными или не содержащими калий, у него возникают:
- сердечные патологии;
- вялость;
- сонливость (даже после хорошего отдыха);
- утрата аппетита;
- слабость в мышцах;
- болезни суставов.
Если соблюдать изнуряющие диеты, не вводить в рацион пищу, богатую K, в организме могут развиться тяжелые патологии.
Эффект от применения калийных удобрений
Калийные удобрения активизируют важнейшие биохимические процессы в тканях и клетках растений, повышают устойчивость культур к различным заболеваниям, как в течение вегетационного периода, так и в послеуборочный период. Значительно улучшают лежкость овощей и плодов. Кроме того, при применении данных удобрений:
- у плодовых культур усиливается накопление моносахаров;
- в корнеплодах повышается содержание сахара;
- в картофеле повышается содержание крахмала;
- у злаковых культур утолщаются клетки стенок соломинок, повышается устойчивость хлебов к полеганию;
- у льна, конопли улучшается качество волокна.
1.Общие сведения
Калий – один из ключевых макроэлементов в организме человека. Это вещество, особенно во взаимодействии с натрием, необходимо для регуляции сократительной активности мышц (в т.ч. миокарда), водно-солевого, кислотно-щелочного и энергетического баланса, высшей нервной деятельности, нормальной ферментации и метаболизма, секреторной активности эндокринных желез, функционирования печени и почек. До половины всех солей в организме – соединения калия, и основной их объем содержится во внутриклеточных жидких пространствах.
В отношении всех микро- и макроэлементов, калия в том числе, должен соблюдаться определенный интервал концентрации.
В противном случае как дефицит, так и избыток приводит к развитию тяжелых, порой жизнеугрожающих состояний. Гиперкалиемия, т.е. чрезмерное содержание калия – типичный тому пример.
Подкормка калийными удобрениями по культурам
Огурцы
Огурцы нуждаются в калии. Калийсодержащие удобрения вносят три раза: первый при посеве, второй раз — при появления 2-3 листочков, третий раз — во время обильного цветения и образования завязей.
Томаты
Томаты не требовательны к калию, предпочитают больше фосфора и азота. Калийные удобрения для томатов разбрасывают вместе с посевом, после высадки рассады в грунт перед цветением проводят вторую подкормку. Можно провести еще одну подкормку в фазе формирования плодов.
При недостатке калия у томатов наблюдается гофрированность и куполообразное закручивание листьев – «краевой запал». Плоды покрываются желтовато-бронзовыми пятнышками.

Нехватка калия в огурцах и томатах
Виноград
Виноград требователен к калию. Если виноград не получает достаточно калия, то он может оттягивать калий из более старых листьев, перенаправляя его к молодым побегам. Плодоносящие кусты винограда ежегодно забирают для роста и формирования плодов до 10-12 г калия.
Взаимодействие калийных удобрений с почвой
Калийные удобрения хорошо растворимы в воде. При внесении в почву они растворяются в почвенном растворе, а затем вступают во взаимодействие с почвенным поглощающим комплексом по типу обменного (физико-химического), а частично и необменного поглощения.
Обменное поглощение катионов калия почвой составляет небольшую часть от всей емкости поглощения. Реакция обменного поглощения катионов калия почвой обратима.
В результате перехода калия в обменно-поглощенное состояние ограничивается его подвижность в почве и предотвращается вымывание за пределы пахотного слоя, за исключением легких почв с низкой емкостью поглощения. Обменно-поглощенный почвой калий удобрений хорошо доступен растениям.
Вторичные процессы взаимодействия почвенного раствора с почвенным поглощающим комплексом постепенно вытесняют из него катионы калия. Активное участие в таком обмене принимает и корневая система растений благодаря корневым выделениям.
На кислых и сильнокислых почвах (в особенности легкого гранулометрического состава), имеющих в составе ППК обменный водород и алюминий, при внесении калийных удобрений наблюдается заметное подкисление почвенного раствора. Поэтому на таких почвах эффективность калийных удобрений снижается.
Кроме того, дополнительное подкисление почвенного раствора происходит и за счет проявления физиологической кислотности калийных солей. Однако следует отметить, что физиологическая кислотность у калийных удобрений значительно меньше, чем у аммонийных, и проявляется она, как правило, только при длительном применении этих удобрений под калиелюбивые культуры, потребляющие большое количество калия.
Необменный (фиксированный) калий обладает значительно меньшей подвижностью, чем обменно-поглощенный. Переход его в раствор и доступность растениям значительно затруднены.
Фиксация калия удобрений разными почвами в зависимости от их минералогического состава и дозы удобрений может составлять от 14 до 82 % от внесенного количества.
При внесении крупнокристаллических или гранулированных удобрений фиксация калия почвой снижалась на 20-30% из-за меньшего контакта удобрения с почвой.
Размер необменного поглощения калия зависит и от дозы вносимого удобрения. Абсолютное количество фиксированного калия при увеличении дозы калийных удобрений резко возрастает, хотя в процентном отношении к внесенной дозе наблюдается понижение фиксации. Потенциальная способность почвы фиксировать калий очень велика.
При систематическом применении калийных удобрений и положительном балансе калия (т. е. при превышении внесенного калия удобрений над его выносом растениями) в почве повышается содержание как подвижных форм калия (водорастворимый и обменный), так и его фиксированных форм.
В условиях дефицита калийных удобрений (т. е. при отрицательном балансе калия) происходит обратный процесс. По мере расходования растениями доступных форм калия (водорастворимого и обменного) происходит постепенный переход фиксированного калия, а отчасти и калия кристаллической решетки в более подвижные формы. Например, в опыте на суглинистой почве (Англия) за 101 год растения вынесли с урожаями в 3-4 раза больше калия, чем его содержалось в почве в обменной форме.
Физические свойства калия
Калий очень мягкий металл, который легко разрезать обычным ножом. Его твердость по Бринеллю составляет 400 кн/м2 (или 0,04 кгс/мм2). Он имеет объемноцентрированную кубическую кристаллическую решетку (5=5,33 А). Его плотность составляет 0,862 г/см3 (200С). Вещество начинает плавиться при температуре в 63,550С, закипать – при 7600С. Имеет коэффициент термического расширения, который равняется 8,33*10-5 (0-500С). Его удельная теплоемкость при температуре в 200С составляет 741,2 дж/(кг*К) или же 0,177 кал/(г*0С). При той же температуре имеет удельное электросопротивление, равное 7,118*10-8ом*м. Температурный коэффициент электросопротивления металла составляет 5,8*10-15.
Калий образует кристаллы кубической сингонии, пространственная группа I m3m, параметры ячейки a
= 0,5247 нм, Z = 2.
Получение рассматриваемого металла

В наше время калий добывают в лабораториях двумя основными способами. Первый — восстановление его из гидроксида с помощью натрия, который химически еще более активен, чем калий. А второй — получение его из хлорида, тоже с помощью натрия. Если добавить к одному молю гидроксида калия столько же натрия, образуется по одному молю щелочи натрия и чистого калия. Уравнение данной реакции выглядит следующим образом: КОН + Na = NaOH + К. Для проведения реакции второго типа нужно смешать хлорид рассматриваемого металла и натрий в равных молярных пропорциях. В результате этого образуются такие вещества, как кухонная соль и калий в одинаковом соотношении. Выразить данное химическое взаимодействие можно с помощью такого уравнения реакции: КСІ + Na = NaCl + К.
Комплексные минеральные удобрения
Выпускаются двойные (азотно-калийные и фосфорно-калийные) и тройные (азотно-фосфорно-калийные) удобрения.
Калийная селитра
Калийная селитра – в состав входят K2O (44–46%) и азот (13%). Внешне – это небольшие серо-белые кристаллы с желтым оттенком, растворимые в воде. Может использоваться даже после образования завязей, так как небольшое количество азота укрепит культуру, но не подстегнет активный рост вегетативной массы.
Калийная селитра чаще всего используется для подкормки корнеплодов (моркови и свеклы) и ягодных культур, подходит для томатов. Вносить удобрение можно в сухом и жидком виде. Последнюю подкормку проводят не менее чем за 3–4 недели до снятия урожая.
Калимагнезия
Калимагнезия – комплексное калийно-магниевое удобрение, без хлора, гигроскопична, не слеживается. Применяют в виде подкормки (10 г/м2) при низком содержании в почве подвижного магния.
Используется для подкормки картофеля.
Нитроаммофоска
Содержание азота, фосфора и калия приблизительно равное. Применяется при основном внесении (вразброс или локально) и припосевном внесении, а так же для некорневой подкормки.
Для чего полезен калий?

Калий участвует во всех критически важных процессах в организме.
- Поддерживает необходимый для тела уровень магния, который жизненно важен для нормальной работы сердца и ряда других процессов.
- Вместе с натрием и хлором является активным участником водно-солевого обмена в организме – обеспечивает функционирование жидкостей в нашем теле и поддерживает осмотическое давление на должном уровне.
- Наряду с кальцием, натрием и магнием принимает участие в кислотно-щелочном равновесии тела, то есть, способствует его ощелачиванию.
- Помогает глюкозе превращаться внутри нас в энергию, а она, в свою очередь, поступает в переработанном виде к мышцам, активизирует их сокращение и является профилактикой паралича.
- Поддерживая энергетический уровень тела, повышает нашу выносливость и обеспечивает силу, а также предотвращает появление хронической усталости.
- Отвечает за регулирование артериального давления и сердечного ритма.
- Участвует в транспортировке нервных импульсов по нервной системе.
- Способствует выведению из тела жидкостей, а, значит, избавляет его от отеков, помогает нормальному мочеиспусканию, поддерживает работу почек.
- В связи с предыдущим пунктом помогает нашему организму освобождаться от шлаков.
- Активизирует мозговое кровоснабжение – насыщает этот жизненно важный орган кислородом и, следовательно, улучшает его деятельность.
Как видите, влияние калия на организм человека очень велико, а потому его дефицит может плачевно отразиться на большом количестве наших органов и систем.
К содержанию
Получение
Минеральные формы чистого сульфата калия относительно редки. Минерал арканит (англ. Arcanite) состоит из чистого K2SO4, представляет собой белые или прозрачные кристаллы, встречается в Калифорнии (США).
Есть много минералов, содержащих соли калия:
- Каинит — MgSO4·KCl·H2O
- Глазерит — 2K2SO4·Na2SO4
- Шёнит — K2SO4·MgSO4·6H2O
- Леонит — K2SO4·MgSO4·4H2O
- Лангбейнит — K2SO4·2MgSO4
- Полигалит — K2SO4·MgSO4·2CaSO4·2H2O
- Сингенит — K2SO4·CaSO4·H2O
Промышленные методы получения основаны на обменных реакциях KCl с различными сульфатами и в результате сульфат калия, как правило, сильно загрязнён побочными продуктами:
- 2KCl + 2MgSO4 ⇄ K2SO4 ⋅ MgSO4 + MgCl2
- K2SO4 ⋅ MgSO4 + 2KCl ⇄ 2K2SO4 + MgCl2
- 2KCl + Na2SO4 ⇄ K2SO4+ 2NaCl
- 2KCl+ CaSO4 ⋅ 2H2O ⇄ K2SO4 + CaCl2 + 2H2O
- 2KCl + FeSO4 ⇄ K2SO4 + FeCl2
Наиболее чистый продукт получают, обрабатывая твёрдый хлорид калия концентрированной серной кислотой:
- 2KCl + H2SO4 →>100oC K2SO4 + 2HCl↑
Прокаливанием с углём минерала лангбейнита:
- K2SO4 ⋅ 2MgSO4 + 2C →>T K2SO4 + 2Mg↓ + 2CO2↑ + 2SO2↑
В лабораторной практике применяют следующие методы:
из оксида калия:
- K2O + H2SO4 → K2SO4 + H2O
вытеснением из слабых или неустойчивых кислот:
- K2CO3 + H2SO4 → K2SO4 + CO2↑ + H2O
из щёлочи и разбавленной кислоты:
- 2KOH + H2SO4 → K2SO4 + 2H2O
из гидросульфата калия:
- 2KHSO4 →240oC K2SO4 + H2SO4
- KHSO4 + KOH → K2SO4 + H2O
- 2KHSO4 + KCl →500oC K2SO4 + HCl↑
окислением сульфида калия:
- K2S + 2O2 →>500oC K2SO4
из надперекиси калия:
- 2KO2 + S →140oC K2SO4
- 2KO2 + SO2 →100oC K2SO4 + O2
Сульфат калия получается при нагреве сульфита калия до температуры в 600 °C:
- 4K2SO3 →600oC K2S + 3K2SO4
Окисление серы бихроматом калия:
- K2Cr2O7 + S →800−1000oC Cr2O3 + K2SO4
Взаимодействием сульфата аммония и гидроксид калия:
- (NH4)2SO4 + 2KOH → K2SO4 + 2NH3↑ + 2H2O
Пищевые источники калия
Калий в основном содержится в растительных продуктах, однако некоторые виды животных продуктов могут быть источником калия. Наиболее богаты калием такие продукты, как: петрушка, курага, сухое молоко, шоколад, различные орехи (особенно миндаль и фисташки), картофель, бананы, авокадо, соя, отруби. Также калий присутствует в значительном количестве в большинстве фруктов, овощей, мясе и рыбе.
Необходимо помнить, что в организме существует определенный баланс между калием и натрием. Если он был нарушен (чаще всего наблюдается дефицит калия), то прием продуктов — источников калия приводит к увеличению выведения натрия, и наоборот.
При потреблении в основном продуктов животного происхождения человек сразу получает калий и натрий уже в сбалансированном соотношении.
Элемент калий и его обозначение
Калий — это химический элемент системы элементов, придуманной Дмитрием Менделеевым, который находится в первой группе. Он имеет атомный номер 19 и атомную массу равную 39,098 г/моль. По своим физическим свойствам элемент представляет из себя металл серебристо-белого цвета. Он очень пластичный и плавкий. Имеет характерный металлический блеск. Калий легко режется ножом и по твердости не уступает куску твердого сыра. Калий состоит из трех изотопов: 39К, 41К, 40К. Два первых соединения являются стабильными, а третий считается достаточно слабым, но при всем этом радиоактивным. Период полураспада последнего соединения составляет 1,32*109 лет. Химический элемент в химии обозначают «К».

В нормальных условиях калий находится в твердом агрегатном состоянии. Температура плавления элемента равна 63 градуса, чего легко добиться при обычном нагревании. Температура же кипения элемента гораздо выше и составляет 761 градус.
Нахождение в природе
Ввиду высокой химической активности калий в свободном состоянии в природе не встречается. Породообразующий элемент, входит в состав слюд, полевых шпатов и т. д. Также калий входит в состав минералов сильвина KCl, сильвинита KCl·NaCl, карналлита KCl·MgCl2·6H2O, каинита KCl·MgSO4·6H2O, а также присутствует в золе некоторых растений в виде карбоната K2CO3 (поташ). Калий входит в состав всех клеток (см. ниже раздел ). Кларк калия в земной коре составляет 2,4 % (5-й по распространённости металл, 7-й по содержанию в коре элемент). Средняя концентрация в морской воде — 380 мг/л.
Месторождения
Крупнейшие месторождения калия находятся на территории Канады (производитель PotashCorp), России (ПАО «Уралкалий», г. Березники, г. Соликамск, Пермский край, Верхнекамское месторождение калийных руд), Белоруссии (ПО «Беларуськалий», г. Солигорск, Старобинское месторождение калийных руд).
Биологическая роль[ | код]
Калий — важнейший биогенный элемент, особенно в растительном мире. При недостатке калия в почве растения развиваются очень плохо, уменьшается урожай, поэтому около 90 % добываемых солей калия используют в качестве удобрений.
Калий в качестве катиона наряду с катионами натрия является базовым элементом так называемого натрий-калиевого насоса клеточной мембраны, который играет важную роль в проведении нервных импульсов.
Калий в организме человека | код
Калий содержится большей частью в клетках, до 40 раз больше, чем в межклеточном пространстве. В процессе функционирования клеток избыточный калий покидает цитоплазму, поэтому для сохранения концентрации он должен нагнетаться обратно при помощи натрий-калиевого насоса. Калий и натрий между собой функционально связаны и выполняют следующие функции:
- Создание условий для возникновения мембранного потенциала и мышечных сокращений.
- Поддержание осмотической концентрации крови.
- Поддержание кислотно-щелочного баланса.
- Нормализация водного баланса.
Рекомендуемая суточная доля калия составляет для детей от 600 до 1700 миллиграммов, для взрослых — от 1800 до 5000 миллиграммов. Потребность в калии зависит от массы тела, физической активности, физиологического состояния и климата места проживания. Рвота, продолжительные поносы, обильное потение, использование мочегонных повышают потребность организма в калии.
Основными пищевыми источниками являются бобы (в первую очередь белая фасоль), шпинат и капуста кормовая, финики, картофель, батат, сушёные абрикосы, дыня, киви, авокадо, помело, бананы, брокколи, печень, молоко, ореховое масло, цитрусовые, виноград. Калия достаточно много в рыбе и молочных продуктах.
Практически все сорта рыбы содержат более 200 мг калия на 100 г. Количество калия в разных видах рыбы различается.
Овощи, грибы и травы также содержат много калия, однако в консервированных продуктах его уровень может быть гораздо меньше. Много калия содержится в шоколаде.
Всасывание происходит в тонком кишечнике. Усвоение калия облегчает витамин B6, затрудняет — алкоголь.
При недостатке калия развивается гипокалиемия. Возникают нарушения работы сердечной и скелетной мускулатуры. Продолжительный дефицит калия может быть причиной острой невралгии.
При избытке калия развивается гиперкалиемия, для которой основным симптомом является язва тонкого кишечника. Настоящая гиперкалиемия может вызвать остановку сердца.
История открытия
Атомный номер калия 19, что указывает на его расположение в химической таблице Менделеева.
Примерная молярная масса 39,1 г/моль.
Электронная конфигурация калия 1s22s22p63s23p64s1

Единственная возможная степень окисления +1 (плюс один).
На внешнем энергетическом уровне имеется всего 1 электрон. Это значит, что максимальная валентность элемента 1.
Кристаллическая решётка простого вещества кубическая объёмно-центрированная.
В 1807 году английский химик Х. Дэви опытным путём получил потассий (латинское название — потассиум). Именно так изначально был назван калий. Проводя электролиз каустической воды и расплавов поташа, учёный заметил образование мягкого легкоплавкого металла. Такое достижение подтолкнуло его к новым открытиям и он стал изучать химические и физические свойства нового вещества.
Такая сенсация потрясла весь научный мир и зарубежные коллеги решили не оставаться в стороне. Уже через 2 года британский эксперт Л. В. Гилберт предложил название «Аль-кали», что в переводе с арабского означает «зола растений». И это не удивительно, ведь золу, которая оставалась после сжигания растений, обрабатывали водой, а полученную смесь выпаривали до сухого остатка. В далёкие времена это использовали как моющее средство. В 1831 году немецкий физик Г. И. Гесс, изучавший свойства нового вещества, предложил своё название для элемента, который также называли «Аль-калий».
Взаимодействие с комплексными соединениями
Калий способен реагировать с кислотами, солями, основаниями и оксидами. С каждым из перечисленных соединений калий вступает в реакцию по разному.
Реакция с водой
Если поместить кусочек калия в воду можно отметить бурную химическую реакцию. Калий, в буквальном смысле слова, будет провоцировать процесс кипения. В результате реакции образуется щелочь и чистый водород.

Реакция с кислотой
Взаимодействие с кислотами в данном случае можно назвать реакцией замещения, так как калий замещает атомы гидрогена из их соединений. В качестве примера можно привести реакцию калия с соляной кислотой. По такому же принципу калий реагирует с другими неорганическими кислотами.
Реакция с оксидами
Эта реакция относится к реакции обмена. Если металл в составе оксида оказывается слабее, чем калий, то элемент вытесняет его из соединения, присоединяя кислород.
Реакция с основаниями
Реакция с основаниями происходит по тому же принципу, что и взаимодействие с оксидами. Калий способен реагировать с соединениями, в которых элемент слабее, чем он сам. В результате данной реакции барий выпадает в осадок.

Реакция с солями
Химическая реакция с солями позволяет получать чистые металлы без примесей. Калий как сильный восстановитель вытесняет более слабый металл, присоединяя остаток соли к себе.
Элемент калий и его обозначение
Калий — это химический элемент системы элементов, придуманной Дмитрием Менделеевым, который находится в первой группе. Он имеет атомный номер 19 и атомную массу равную 39,098 г/моль. По своим физическим свойствам элемент представляет из себя металл серебристо-белого цвета. Он очень пластичный и плавкий. Имеет характерный металлический блеск. Калий легко режется ножом и по твердости не уступает куску твердого сыра. Калий состоит из трех изотопов: 39К, 41К, 40К. Два первых соединения являются стабильными, а третий считается достаточно слабым, но при всем этом радиоактивным. Период полураспада последнего соединения составляет 1,32*109 лет. Химический элемент в химии обозначают «К».

В нормальных условиях калий находится в твердом агрегатном состоянии. Температура плавления элемента равна 63 градуса, чего легко добиться при обычном нагревании. Температура же кипения элемента гораздо выше и составляет 761 градус.
История и происхождение названия
Соединения калия используются с древнейших времён. Так, производство поташа (который применялся как моющее средство) существовало уже в XI веке. Золу, образующуюся при сжигании соломы или древесины, обрабатывали водой, а полученный раствор (щёлок) после фильтрования выпаривали. Сухой остаток, помимо карбоната калия K2CO3, содержал сульфат калия K2SO4, соду и хлорид калия KCl.
19 ноября 1807 года в Бейкеровской лекции английский химик Дэви сообщил о выделении калия электролизом расплава едкого кали (KOH) (в рукописи лекции Дэви указал, что он открыл калий 6 октября 1807 года). Дэви назвал его «потасий» (лат. potasium); это название (правда, в некоторых языках с двумя буквами s) до сих пор употребительно в английском, французском, испанском, португальском и польском языках. При электролизе влажного едкого кали KOH на ртутном катоде он получил амальгаму калия, а после отгонки ртути — чистый металл. Дэви определил его плотность, изучил химические свойства, в том числе разложение воды и поглощение водорода.
В 1808 году французские химики Гей-Люссак и Л. Тенар выделили калий химическим путём — прокаливанием KOH с углём.
В 1809 году немецкий физик Л. В. Гильберт предложил название «калий» (лат. kalium, от араб. аль-кали — поташ). Это название вошло в немецкий язык, оттуда в большинство языков Северной и Восточной Европы (в том числе русский) и «победило» при выборе символа для этого элемента — K.
Биологическая роль калия
Калий вместе с другими важнейшими электролитами обеспечивает необходимое осмотическое давление в биологических жидкостях организма и в клетках, является компонентом буферных систем, поддерживает электрический потенциал на мембранах клеток всех тканей.
Главная биологическая функция калия — формирование совместно с другими электролитами (натрий, хлор) разницы потенциалов на мембранах клеток и передача ее изменения по клеточной мембране, за счет обмена с ионами натрия, что особенно важно для нервных и мышечных клеток. Это обуславливает постоянное присутствие в клетках натрия, хлора и калия
В организме эти элементы содержатся в определенном соотношении, обеспечивая гомеостаз (постоянство внутренней среды). Нарушение равновесия между калием и натрием ведет к патологии водного обмена, обезвоживанию, мышечной слабости.
Главные преимущества калия
Каждый раз исследования, посвященные этому минералу, подтверждают его жизненно важную роль для человека. Снова и снова ученые напоминают: дефицит К ведет к гипертонии, инсульту, диабету, подагре, остеопорозу, ревматизму, болям в сердце и кишечнике. В медицине известны случаи, когда калий-дефицит провоцировал значительное ухудшение памяти.
Активизирует работоспособность мозга
К-дефицит, в первую очередь, сказывается на работоспособности мозга. Это объясняется тем, что минерал помогает снабжать мозговые клетки кислородом, без которого функциональность органа резко снижается. Первые признаки нехватки макроэлемента – быстрая утомляемость и неспособность сконцентрироваться на важных вещах. Такое состояние обычно продолжается до устранения калий-дефицита.
Защищает сердце от болезней
Адекватное потребление калия защитит от риска развития сердечных болезней и инсульта. Этот нутриент способен регулировать кровяное давление и частоту сердцебиения, а значит, уменьшать нагрузку на артерии и сердечную мышцу
Важно, что многие продукты, содержащие К, являются прекрасными источниками антиоксидантов, благотворно влияющих на работу сердца и всего организма
Укрепляет мышцы
Калий играет важную роль в работе укрепления мышц
Желаете нарастить мускулы или просто поддерживать их здоровье – обратите внимание на продукты, богатые этим минералом. Бананы, авокадо, изюм и курага на клеточном уровне влияют на состояние мышц
Калий, содержащийся в них, способствуют более быстрому восстановлению мускулатуры, поддержанию ее в тонусе.
Регулирует уровень жидкости
Суточная норма калия позволяет поддерживать баланс жидкости в организме, а это необходимо для обеспечения работоспособности всех систем, поддержания стабильного веса и объемов тела. Этой способностью К напоминает кальций и натрий, в «обязанности» которых также входит контроль за водным балансом в организме.
Стабилизирует артериальное давление
Тревожит повышенное давление? Возможно, вам не хватает калия. Этот макроэлемент способен расслаблять сосуды, благодаря чему снижается напор кровотока в артериях. Продукты, богатые калием, помогут бороться с гипертензией людям, страдающим диабетом, находящимся в зоне риска возникновения инсультов или сердечных приступов.
Укрепляет кости
Не только кальций и фтор являются элементами, важными для здоровья костей. Роль калия нельзя недооценивать. Человеческое тело – это множество систем и подсистем, работающих в комплексе. Для поддержания функциональности организма необходим полный набор микро- и макроэлементов. В частности, здоровье костной ткани зависит от баланса нескольких минералов, в том числе и калия. Регулярное потребление продуктов, богатых этим макровеществом, защитит от развития остеопороза.
Минерал-антистресс
От здоровья нервной системы напрямую зависит функционирование всего организма, самочувствие человека. Не последнюю роль для нервных клеток играет калий. Повышенное напряжение и нервозность также могут быть сигналом о дефиците К. Недостаток минерала снижает способности организма бороться со стрессами, что со временем может перерасти в гипертонию и серьезные нарушения в работе нервной системы.
Ускоряет метаболизм
Строго придерживаетесь низкокалорийной диеты, а лишний вес все не уходит? Не исключено, что таким образом организм сигнализирует о недостаточном потреблении калия. Нехватка макроэлемента замедляет метаболические процессы. Он помогает организму расщеплять и усваивать пищу, усиливает работу других минералов, важных для адекватного хода обменных процессов. Пересмотрите свой диетический рацион, дополнив его калийсодержащими продуктами, и, возможно, снижение веса не заставит себя долго ждать.
Снимает спазмы в мышцах
 Именно калий является тем минералом, нехватка которого проявляется мышечными спазмами и судорогами. Даже малейший дисбаланс минерального состава проявляется болями и дискомфортом в мышцах.
Именно калий является тем минералом, нехватка которого проявляется мышечными спазмами и судорогами. Даже малейший дисбаланс минерального состава проявляется болями и дискомфортом в мышцах.
Роль для почек
А вот во взаимосвязи между калием и почками не все так просто. С одной стороны, он является важным нутриентом, снижающим риск развития мочекаменной болезни, так как соли калия способны уменьшать кислотность в кровотоке. А с другой стороны, есть категория людей, которым категорически запрещается употреблять калия без врачебного контроля. Это люди, страдающие почечной недостаточностью. У них на фоне болезни формируется гиперкалиемия, пренебрежение которой может стать причиной внезапной остановки сердца.
Физические свойства

Калий под слоем ТГФ Калий — серебристый металл с характерным блеском на свежеобразованной поверхности. Очень лёгок и легкоплавок. Относительно хорошо растворяется в ртути, образуя амальгамы. Будучи внесённым в пламя горелки, калий (а также его соединения) окрашивает пламя в характерный розово-фиолетовый цвет.

Калий активно взаимодействует с водой. Выделяющийся водород воспламеняется, а ионы калия придают пламени фиолетовый цвет. Раствор фенолфталеина в воде становится малиновым, демонстрируя щелочную реакцию образующегося KOH
Калий образует кристаллы кубической сингонии, пространственная группа I m
3m , параметры ячейкиa = 0,5247 нм,Z = 2.
Строение калия и его физико-химические свойства
Химический элемент располагается в четвертом периоде, поэтому все его электроны будут расположены на четырех энергетических уровнях. Энергетическая формула элемента выглядит следующим образом: +19К: 2ё; 8ё; 8ё; 1ё.Графическая формула элемента выглядит соответствующим образом.
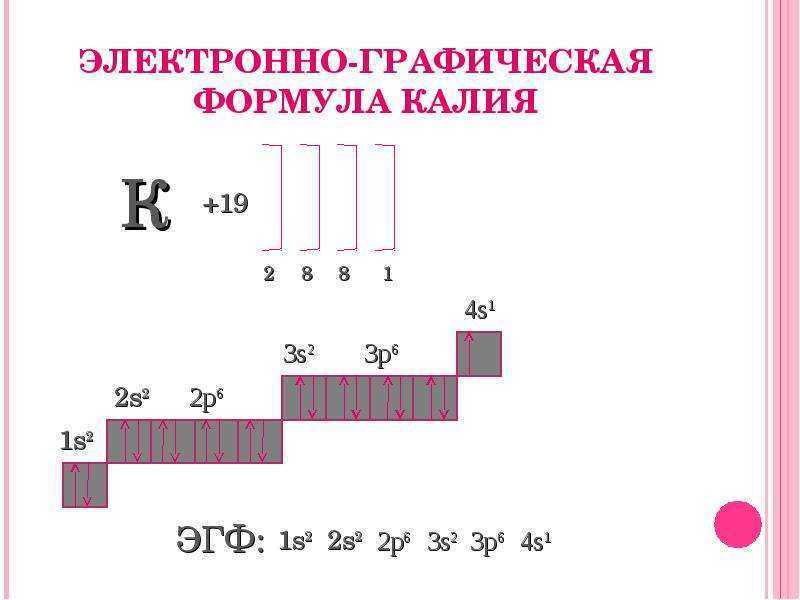
Исходя из электронного строения элемента, можно сделать вывод, что калий имеет валентность равную I. Так как в химических реакциях элемент отдает один электрон с внешнего энергетического уровня, он проявляет восстановительные свойства, приобретая степень окисления +1.
Благодаря своему расположению в таблице Менделеева, можно сказать, что восстанавливающие свойства калия выражены гораздо сильнее, чем у Na, но слабее, чем у Rb. Такая закономерность связана с увеличением атомного диаметра. Кроме этого, калий будет сильнее, чем атом кальция, так как на внешнем энергетическом уровне у кальция уже два электрона и оторвать их гораздо сложнее, чем один.
Калий по своей химической структуре является простым веществом с металлической кристаллической решеткой и металлической химической связью. Исходя их этого, можно сказать, что калий легко вступает в реакцию и очень быстро окисляется на воздухе.
Калий, свойства атома, химические и физические свойства.
K 19 Калий
39,0983(1) 1s2 2s2 2p6 3s2 3p6 4s1
Калий — элемент периодической системы химических элементов Д. И. Менделеева с атомным номером 19. Расположен в 1-й группе (по старой классификации — главной подгруппе первой группы), четвертом периоде периодической системы.
Атом и молекула калия. Формула калия. Строение калия
Изотопы и модификации калия
Свойства калия (таблица): температура, плотность, давление и пр.
Физические свойства калия
Химические свойства калия. Взаимодействие калия. Реакции с калием
Получение калия
Применение калия
Таблица химических элементов Д.И. Менделеева